Par: K. S. Jayaraman
Envoyer à un ami
Les coordonnées que vous indiquez sur cette page ne seront pas utilisées pour vous envoyer des emails non- sollicités et ne seront pas vendues à un tiers. Voir politique de confidentialité.
- La génomique : la génétique, en plus grand
- Que de promesses !
- Analyser les analyses
- Au-delà du séquençage
- Des histoires vraies
- Ne négligez pas les questions d'éthique
Comment réconcilier la génomique en santé et le journalisme scientifique ? Les conseils de K.S. Jayaraman pour répondre aux questions pertinentes, tout en évitant l'écueil de l'hyperbole médiatique.
Il y a dix ans déjà, des chercheurs dévoilaient une ébauche de la séquence du génome humain. Le Président Bill Clinton déclarait alors que ce succès "révolutionnerait le dépistage, la prévention et le traitement de la plupart, sinon de toutes les maladies humaines".
Nous n'y sommes peut-être pas encore. Pourtant, au regard des avancées fulgurantes de la recherche dans le monde entier de cette décennie écoulée, la génomique offre de plus en plus de sujets d'investigation au journaliste scientifique ou médical.
Toutefois, le traitement journalistique de la génomique dépasse le simple fait de rédiger un article sur la science ou la médecine. Des questions comme l'éthique, la vie privée et la propriété intellectuelle, toutes aussi difficiles, s'y entremêlent. Voici donc quelques conseils pratiques pour vous tirer d'affaire.
La génomique : la génétique, en plus grand
Le génome est l'ensemble de l'information génétique codée dans l'ADN d'un organisme (on parle d'ARN dans le cas des virus). Les génomes comprennent à la fois des gènes — fragments d'ADN qui codent pour des protéines spécifiques — mais également des séquences non codantes qui se situent entre les gènes.
Si la recherche en génétique se focalise sur un seul gène à la fois, la génomique étudie des génomes entiers et ausculte l'interaction entre les gènes. Elle peut couvrir tous les domaines la recherche biologique. Ces conseils se limiteront toutefois à la génomique relative à la santé humaine et à la médecine.
Or, même si l'on en réduit la portée à un seul domaine, la génomique peut avoir plusieurs applications.
Ainsi, peut-être faîtes vous un reportage sur une étude qui procède au séquençage du génome d'un agent pathogène, avec pour objectif de comprendre comment il cause une maladie humaine. Autre exemple, des études de l'associationà l'échelle du génome peuvent chercher à comprendre comment la variation du génome humain au sein et entre des populations influe sur l'apparition et l'évolution des maladies.
Votre reportage peut également concerner la médecine personnalisée, un nouveau champ de recherche qui étudie le génome d'un individu afin de prédire le risque de pathologies ou déterminer les médicaments les plus indiqués.
Il vous faudra donc bien comprendre la génomique et son champ d'application. Pour commencer, les fiches d'information (en anglais) de l'Institut national de Recherche sur le Génome humain des Etats-Unis (US National Human Genome Research Institute) sur la science et l'éthique de la génomique peuvent vous être utiles.
Que de promesses !

L'ADN en laboratoire : les scientifiques peuvent étudier des génomes entiers.
Flickr/Gravitywave
La génomique offre le potentiel d'une amélioration de la santé dans les pays en développement. Pour la première fois, des médecins et des chercheurs peuvent étudier des génomes entiers afin de déterminer une éventuelle vulnérabilité à des pathologies, ou étudier le génome d'un agent pathogène pour déterminer de nouvelles cibles de vaccins et de médicaments.
L'avènement de la génomique a certainement suscité l'espoir de découverte de traitements contre le cancer, le diabète, la maladie d'Alzheimer et les cardiopathies. Pourtant, de nombreuses questions restent en suspens et il faudra probablement attendre des décennies pour que cette promesse soit tenue.
Il est donc important de ne pas sur-médiatiser votre article en suscitant de faux espoirs. Ne faites pas non plus fi des problèmes restant à résoudre, pour que les résultats des recherches puissent être intégrés à de nouveaux traitements ou de nouvelles techniques (comme les kits de diagnostic).
Dix ans après l'ébauche de la séquence du génome humain, la 'révolution médicale' annoncée ne s'est pas concrétisée, et ce même dans les pays développés (voir une série d'articles parue dans Nature à l'occasion du dixième anniversaire). Par ailleurs, dans un récent sondage auprès de plus de 1 000 biologistes, la majorité estime que ces promesses ne seront tenues qu'après plusieurs décennies.
Lors de votre prochain reportage sur la découverte d'une série de gènes associés à une maladie donnée, prenez donc le temps de vous interroger sur la véritable portée de cette avancée.
Certes, ces découvertes pourraient permettre de mettre au point de nouveaux tests ou de nouveaux traitements. Mais interrogez les chercheurs : ces recherches pourraient être utiles en clinique ? A quelle échéance ? Dans un deuxième temps, discutez avec votre rédacteur en chef de l'angle, voire même de la nécessité de couverture de cet événement. En effet, si cette découverte pourrait intéresser les chercheurs, est-ce là vraiment votre public cible ? Dans le cas contraire, votre article pourrait manquer de pertinence aux yeux de celui-ci.
Analyser les analyses
Le séquençage du génome, méthode permettant de déterminer l'ordre des nucléotides qui constituent l'ADN, coûte de moins en moins cher. Les laboratoires proposant un séquençage partiel ou intégral du génome humain poussent comme des champignons. Elles prétendent, entre autres affirmations, que ce type de test donne aux individus une idée de leur niveau d'exposition à certaines pathologies.
Toutefois, les réponses sont rarement précises. Certes, un test génétique de dépistage de la chorée de Huntington, une maladie causée par une seule anomalie génétique peut donner un résultat négatif ou alors révéler un risque réel.
Mais, d'autres pathologies comme les cardiopathies ou la maladie d'Alzheimer peuvent être causées par plusieurs gènes qui interagissent. L'analyse génomique ne permettrait de déterminer que si vous êtes plus exposé à la maladie que le reste de la population. Admettons qu'un individu découvre qu'il a un risque de contracter la maladie d'Alzheimer de sept pour cent supérieur de la moyenne ? Que ferait-il avec une telle information ?
Les services d'analyse génétique se multiplient à un rythme que les organes de régulation ne peuvent suivre. En 1993, il existait des tests pour environ 100 maladies. En 2009, leur nombre s'élevait à environ 1 900, et même dans des pays comme les États-Unis ce secteur est très peu régulé. Votre pays a-t-il les moyens d'en assurer la régulation ?
L'Inde compte au moins une douzaine de laboratoires proposant des tests de prédisposition génétique. Cependant, ce pays ne dispose d'aucune agence de régulation de ces analyses ou d'accréditation des laboratoires. Aux États-Unis, le Bureau de Comptabilité générale (General Accounting Office) a conclu en juillet 2010 que les résultats de certains tests génétiques prédictifs directement disponibles au consommateur étaient "propres en induire en erreur et presque inutiles".
D'autres au contraire estiment que ces analyses permettent aux consommateurs de prendre leur santé en main. Ainsi, demandez l'avis d'un spécialiste sur un nouveau test ou service avant d'en parler dans un article. Ne laissez pas la frénésie que suscite la génomique faire de vous le portevoix des relations publiques d'une entreprise.
Et si vous rédigez un article sur l'utilisation de tests génétiques pour des affections chroniques comme les cardiopathies, n'oubliez pas que les gènes ne représentent qu'un seul aspect du problème. Il est vrai qu'ils sont déterminants dans la prédisposition à une maladie, mais les facteurs liés à l'environnement, comme le régime alimentaire, ont souvent un impact considérable.
Au-delà du séquençage
Le séquençage intégral du génome étant désormais relativement peu onéreux et rapide, il semble que la presse annonce chaque semaine que les 'codes' d'agents pathogènes et de leurs vecteurs ont été 'décryptés'.
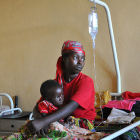


Un fossé génomique se creuse-t-il entre pays développés et pays en développement ?
UN Development Programme
Mais les séquences à elles seules ne représentent plus un événement médiatique. Recherchez plutôt du côté des résultats utiles qui découlent de la séquence. Ainsi, comment les chercheurs indiens espèrent-t-ils utiliser le génome du Mycobacterium tuberculosis pour mettre aupoint de nouveaux médicaments ?
Enquérez-vous des perspectives auprès des chercheurs. Que faut-il faire pour tirer profit des données génomiques ? Quels en sont les applications potentielles ? Les chercheurs ont-ils établi une séquence génétique (l'ordre de tous les acides nucléiques de l'ADN) ou alors une carte génétique (une représentation de 'repères' génétiques comme les gènes) ? Vous pourriez conclure qu'une nouvelle séquence ne présente pas d'intérêt médiatique une fois les réponses à ces questions obtenues.
Et si un chercheur vous affirme qu'il faudra trois ans pour identifier la base génétique d'une pathologie à partir d'une séquence, revenez le voir au bout de cette période. Vous éviterez ainsi que votre article ne devienne simplement une longue liste de séquences nouvellement découvertes.
Des histoires vraies
Les implications de la génomique pour nos sociétés sont une source de sujets intarissable. Pour ne prendre que quelques exemples : un 'fossé génomique' va-t-il naître entre pays riches et pays pauvres et entre les riches et les pauvres d'un même pays ?
Pourra-t-on convaincre les laboratoires pharmaceutiques —du Nord et du Sud — à recourir aux techniques de la génomique pour mettre au point des traitements et améliorer le dépistage des maladies négligées ? La R&D en santé restera-t-elle axée uniquement sur les besoins des pays riches ?
Faut-il permettre aux entreprises de biotechnologies de breveter les gènes ? Pour certains, le retrait des gènes de la liste des découvertes brevetables ouvrira la recherche scientifique et technique aux pays et chercheurs plus pauvres qui travaillent à l'amélioration de la santé dans les pays en développement. Pour d'autres, une telle décision entraverait la R&D, car les entreprises à but lucratif se détourneraient de ce domaine de recherche. Essayez de suivre ces débats.
Demandez aux chercheurs comment ils entendent aider les pauvres. Les technologies développées suite à leurs travaux seront-elles abordables ? Vous pouvez également demander aux chercheurs s'ils prennent en compte les implications en matière de propriété intellectuelle. Entendent-ils développer eux-mêmes la technologie ou envisagent-ils de céder la licence à une entreprise qui risquerait de fixer un prix prohibitif ?
Si votre pays investit dans la génomique, cherchez à savoir si les coûts sont abordables, ou si ces efforts se font au détriment d'approches traditionnelles (et peut-être plus efficaces) de santé publique.
Pour justifier ses investissements dans la génomique, la Thaïlande a souligné le fait qu'un tiers de sa population est porteur des gènes de la thalassémie, une pathologie héréditaire du sang. La génomique constitue donc, pour les autorités sanitaires thaïlandaises, un outil de dépistage et de traitement de cette maladie.
L'Inde travaille à la création d'un Institut national de Génomique biomédicale (National Institute of Biomedical Genomics) à Kolkata, dans l'optique d'améliorer la santé publique. Cependant, pour certaines personnes en Inde, la génomique n'est pas une priorité. En effet, nombreux sont ceux qui pensent qu'il faudrait accorder la priorité aux efforts de prévention élémentaire et aux soins de santé primaires.
Même si le dépistage génétique peut être nécessaire dans certaines communautés, les consultations génétiques et le traitement après le dépistage pourraient être hors de prix.
C'est là que se situe le nœud du problème. Votre pays a-t-il les moyens de s'offrir les fruits de la médecine génomique ? Vous pourriez demander l'avis des organisations non gouvernementales œuvrant dans les communautés où des échantillons sont prélevés pour des études génomiques.
Ne négligez pas les questions d'éthique
Cherchez également à savoir si votre pays est doté de l'infrastructure éthique pour faire face aux nombreuses implications de la recherche en génomique.
Votre pays pourrait constituer un champ d'expérimentation idéal en génomique. Des chercheurs internationaux pourraient entreprendre des études d'associationà l'échelle du génome. Ils pourraient, ainsi, étudier les marqueurs génétiques associés au diabète dans différents groupes ethniques. Pour ce faire, il faudra des échantillons prélevés sur des centaines voire des milliers de personnes.



Votre pays est-il doté de lois de protection de la vie privée pour gérer l'information génomique ?
Flickr/Shaury
Mais les procédures appropriées de consentement éclairé existent-elles ? La confidentialité peut-elle être garantie ? Les employeurs pourraient-ils utiliser les informations génétiques pour discriminer contre certaines personnes ?
Qu'advient-il de l'information génétique fournie dans le cadre de la recherche ? Demandez aux chercheurs et aux autorités si les recherches ont été autorisées. Existe-t-il des garanties de confidentialité pour les personnes qui contribuent à de telles banques d'ADN dans votre pays ?
Par ailleurs, les participants seront-ils informés des résultats de l'étude ? Les résultats risquent-ils d'être source d'inquiétude, s'il n'y a pas de traitement ou de changement du mode de vie à proposer ?
Si la liste de précautions à prendre est longue, pensez au potentiel cette science. La génomique a de beaux jours devant elle et, au regard de la réduction du coût du séquençage du génome, la quantité des données génomiques est appelée à augmenter.
Ainsi, si vous n'êtes qu'au début de votre carrière, vous avez tout le temps de comprendre la génomique. Et vous ne manquerez pas de sujets à couvrir dans ce domaine passionnant.
Rappelons la conclusion de Francis Collins, directeur de l'Institut national de Recherche sur le Génome humain (National Human Genome Research Institute) : 'le meilleur est à venir'.
K. S. Jayaraman, anciennement correspondant scientifique de Press Trust of India, est un journaliste scientifique indépendant basé à Bangalore, en Inde.
Autres articles sur le thème Santé


Contenu sponsorisé
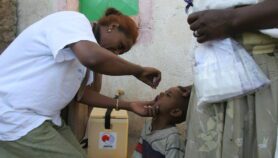
La périlleuse opération de surveillance de la polio dans les zones de conflits
09/12/22